
-
中文 | EN

中文 | EN
发布时间:2023-11-24 00:00:00.0
卵巢癌是妇科肿瘤中致死率最高的癌种,且经常在发现时已进展至晚期。在卵巢癌的临床治疗中,手术和系统性化疗能一定程度地提升生存率,但疗效仍不够理想;另一方面,基于合成致死抑癌机制和PARP抑制剂的靶向疗法仅适用于对部分卵巢癌患者。无论如何,新的卵巢癌治疗药物亟待发现。与其他癌细胞相比,卵巢癌细胞中大量基因的拷贝数异常变化,进而促使多种促癌基因表达上调——这使得卵巢癌的进展极度依赖于基因的转录进程,也为临床治疗提供了可能成药的靶标。

中国科学院上海有机化学研究所生物与化学交叉研究中心、生命过程小分子调控全国重点实验室的谭立课题组曾与仁济医院、上海市妇科肿瘤重点实验室的庄光磊、狄文课题组合作,针对卵巢癌细胞中调控转录延伸过程的关键因子CDK12/13研制了一系列新型激酶抑制剂,并在动物肿瘤模型上取得了很好的抑癌效果。近期,他们又针对卵巢癌细胞中催化mRNA剪接、调控转录终止的CPSF复合物关键组件——CPSF3——研制了新型的小分子抑制剂,并在Science Advances期刊上以共同通讯作者身份发表相关研究论文“Therapeutic targeting of CPSF3-dependent transcriptional termination in ovarian cancer”。
该项研究发现,卵巢癌细胞的增殖极度依赖于转录终止机制,而CPSF3的核酸内切酶活性对于该机制的正常维持不可或缺。在这些生物学发现的基础上,谭立课题组与合作者进行了小分子抑制剂的筛选,旨在进一步验证CPSF3在卵巢癌细胞和动物肿瘤模型中的可成药性。基于一些已报道苯硼酸半酯类化合物特有的抗菌或抗癌活性,研究团队推测,相关化合物的硼酸官能团可能与CPSF3催化位点的锌离子发生络合,进而占据其底物结合口袋实现抑制。通过进一步的理性设计和构效关系研究,研究团队最终获得了高活性、高特异性、可用于活体的HQY426等CPSF3抑制剂。无论是作为单药还是与顺铂或PARP抑制剂联用,HQY426等化合物均在多种卵巢癌细胞和小鼠肿瘤模型上表现出很好的抗癌效果,活性远优于已报道的CPSF3抑制剂。此外,CPSF3催化口袋中氨基酸残基的点突变试验结果进一步表明,HQY426等化合物的药效特异性地来源于其对CPSF3的抑制。
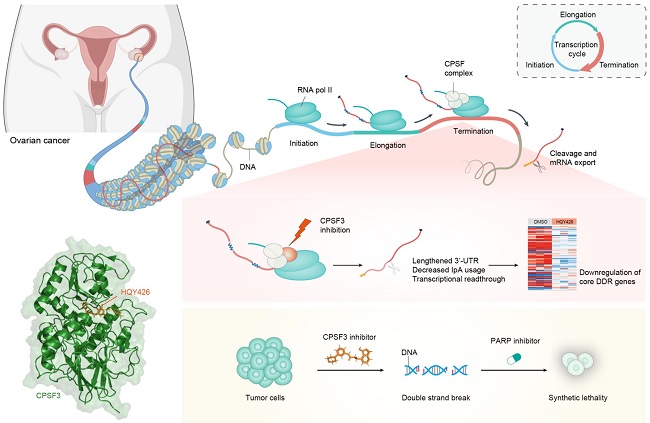
图1. 新型CPSF3抑制剂的发现与应用
总之,这些新型CPSF3抑制剂的发现不但进一步证明了转录终止机制作为卵巢癌临床治疗靶标的成药潜质,同时还为相关靶向抗癌药物的创制提供了极具潜力的先导化合物。当前,研究团队正针对这些抑制剂的成药性质进行进一步优化,同时在临床前研究中进一步拓展其应用场景。该项研究在多个合作课题组支持下,受国家自然科学基金委、上海市科委和中国科学院资助完成。
论文链接:https://www.science.org/doi/10.1126/sciadv.adj0123
