
-
中文 | EN

中文 | EN
发布时间:2025-08-26 00:00:00.0
磷是维持人体生命活动的必需元素,在核酸构成、能量代谢、信号传导及骨骼发育等生理过程中发挥关键作用。细胞内磷酸盐的摄入对生命活动至关重要,但是过量的磷酸盐积累会与钙、镁、铁等离子沉积,带来细胞和组织毒性,需要外排机制及时平衡。XPR1是目前人体唯一已知的磷酸盐外排蛋白,其功能异常与脑钙化、血栓形成、肿瘤发生等多种疾病密切相关。在原发性基底节脑钙化症中,XPR1功能失调导致磷酸盐外排障碍,进而形成钙磷沉积,最终诱发神经系统病变[1]。在细胞内XPR1的功能可被磷酸盐浓度指示分子焦磷酸肌醇InsP8激活[2]。同时,支架蛋白KIDINS220能与XPR1形成复合物调控磷酸盐的外排[3]。但是KIDINS220和InsP8调控XPR1功能的分子机制并不清晰,阻碍了我们对XPR1功能失调引起的脑钙化等疾病发生机理的理解。
近日,中国科学院上海有机化学研究所生物与化学交叉研究中心、生命过程小分子调控国家重点实验室张一小课题组,联合澳大利亚国立大学Ben Corry课题组、上海科技大学孙亚东课题组以及美国国立环境健康科学研究所Stephen Shears课题组,在Molecular Cell杂志上发表了题为“KIDINS220 and InsP8 safeguard the stepwise regulation of phosphate exporter XPR1”的研究文章。该研究通过结构解析、功能研究、计算模拟等手段揭示了XPR1一种精细的“key-to-locks”活性调控方式,以及一种独特的“knock-kiss-kick”磷酸转运外排机制,阐明了原发性脑钙化相关突变的致病机理,并发现了磷酸外排同源蛋白XPR1、PXo、PHO1在进化上的保守性和差异性。

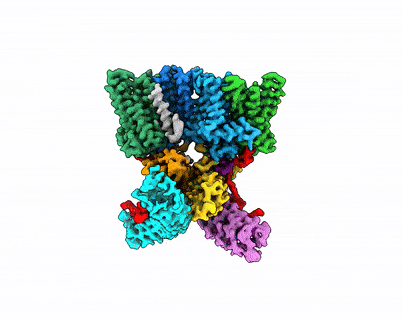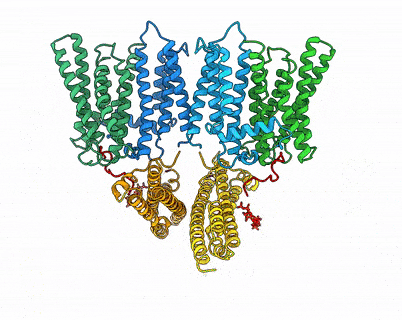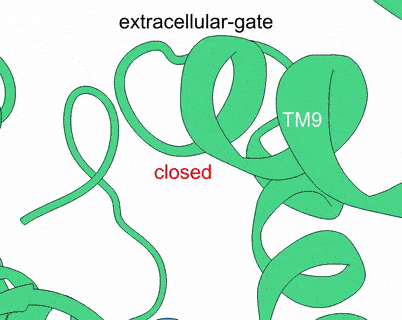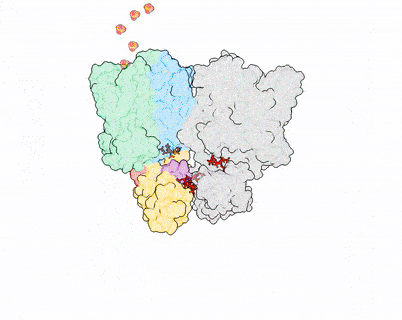
图1. XPR1–KIDINS220复合物结构及InsP8激活XPR1的全构象变化过程
“Key-to-locks”活性调控方式:本研究通过冷冻电镜解析了XPR1与神经元支架蛋白KIDINS220复合物以及XPR1与InsP8复合物的高分辨三维结构,捕捉到XPR1激活过程中的多种功能状态。结合功能实验,本研究发现KIDINS220能将XPR1稳定在关闭状态,存在多重限制机制来给磷酸盐外排活性上“锁”。而天然底物InsP8,这一分子犹如“钥匙”,能够诱发XPR1的逐步激活:(1)在关闭状态中,KIDINS220能够与XPR1的不同基序结合,将XPR1的SPX结构域牢牢锁定在非翻转的关闭状态。其中,XPR1的α1螺旋形成interaction hub来稳定该构象。只有在InsP8存在并与XPR1的α1螺旋结合时,这一限制及其他内部约束才能被解除;(2) 在关闭状态中,XPR1的C-loop形成“盖子”,遮挡住胞内入口。InsP8诱导SPX结构域发生逐步构象重排,并发生180度的大翻转。翻转后的SPX暴露出与C-loop的结合界面,将胞内入口打开,从而解除第二重限制;(3)XPR1的TM9b螺旋控制着外侧出口,当TM9b向外运动并扩大外侧通道时,磷酸基团才能顺利转运至胞外(图1)。综上所述,XPR1的激活需要依次解除由KIDINS220、α1螺旋、C-loop和TM9b螺旋等形成的多重限制,从而实现孔道开放,这一“key-to-locks”机制揭示了XPR1活性的精细调控模式。
“Knock-kiss-kick”磷酸转运外排机制:通过对电镜数据的细致计算分析,研究人员发现XPR1胞内和胞外开口的开放是独立的,捕捉到了磷酸盐外排通道“关/关(内/外),开/关,关/开,开/开”四种不同的构象,这种互不耦联的转运模式与传统的转运蛋白完全不同。值得注意的是,在这四种构象下,在转运通道内部均存在着一处非常狭窄的constriction site,即使是在“开/开”构象下,磷酸盐也难以通过。结合磷酸基团的相互作用分析及分子动力学模拟,研究人员发现了磷酸盐在通道内经历了一个独特的外排过程:磷酸盐首先通过静电互斥,将constriction site附近的负电氨基酸向外推,将“门”敲开(knock),随后在由多个带正电氨基酸构成的磷酸结合口袋内短暂停留(kiss),附近带负电及极性氨基酸平衡上述正电口袋的电性,削弱结合能力,口袋中结合的磷酸盐短暂停留后被下一个进入口袋的磷酸盐向外踢出(kick),最终完成转运。基于此,本研究提出了一种新颖的“knock–kiss–kick”模型,用以描述XPR1介导的磷酸外排机制。
原发性家族性脑钙化症(PFBC)相关突变的致病机理:本研究不仅揭示了XPR1的正常调控机制,还为理解脑疾病提供了分子层面的解释。PFBC患者中常见的致病突变(如R459C、R570L等)[1, 4]位于XPR1通道内的关键识别和门控区域。本研究解析了R459C、R570L这两种突变体的结构,意外发现R459C呈现出类似于InsP8结合的激活态构象特征:SPX发生翻转,胞内侧入口开放;而R570L则稳定于向外开放的构象。然而,这些突变虽然具有XPR1激活开放的构象特征,但是改变了通道内部的环境,使得磷酸盐无法正常结合和转运,显著削弱了外排能力,最终导致钙磷沉积。本研究为由XPR1功能失调引起的脑钙化发病机制提供了直接的分子阐释。
XPR1同源蛋白进化的保守性和差异性:XPR1的同源蛋白PHO1和PXo分别在植物和果蝇中发挥调节磷酸稳态的重要作用。本研究通过结构解析发现,XPR1与PHO1、PXo在结构上高度相似,但也存在显著差异: PXo始终保持外侧开口开放,且InsP6或InsP8均无法使其SPX结构域稳定,这提示PXo可能具有不同的激活调控机制。在解析PHO1结构时,本研究发现其两个单体呈现不对称分布,但这一特征与其功能之间的关系尚需进一步研究。这些结果提示,磷酸外排机制在不同物种中经历了保守与分化的双重进化。
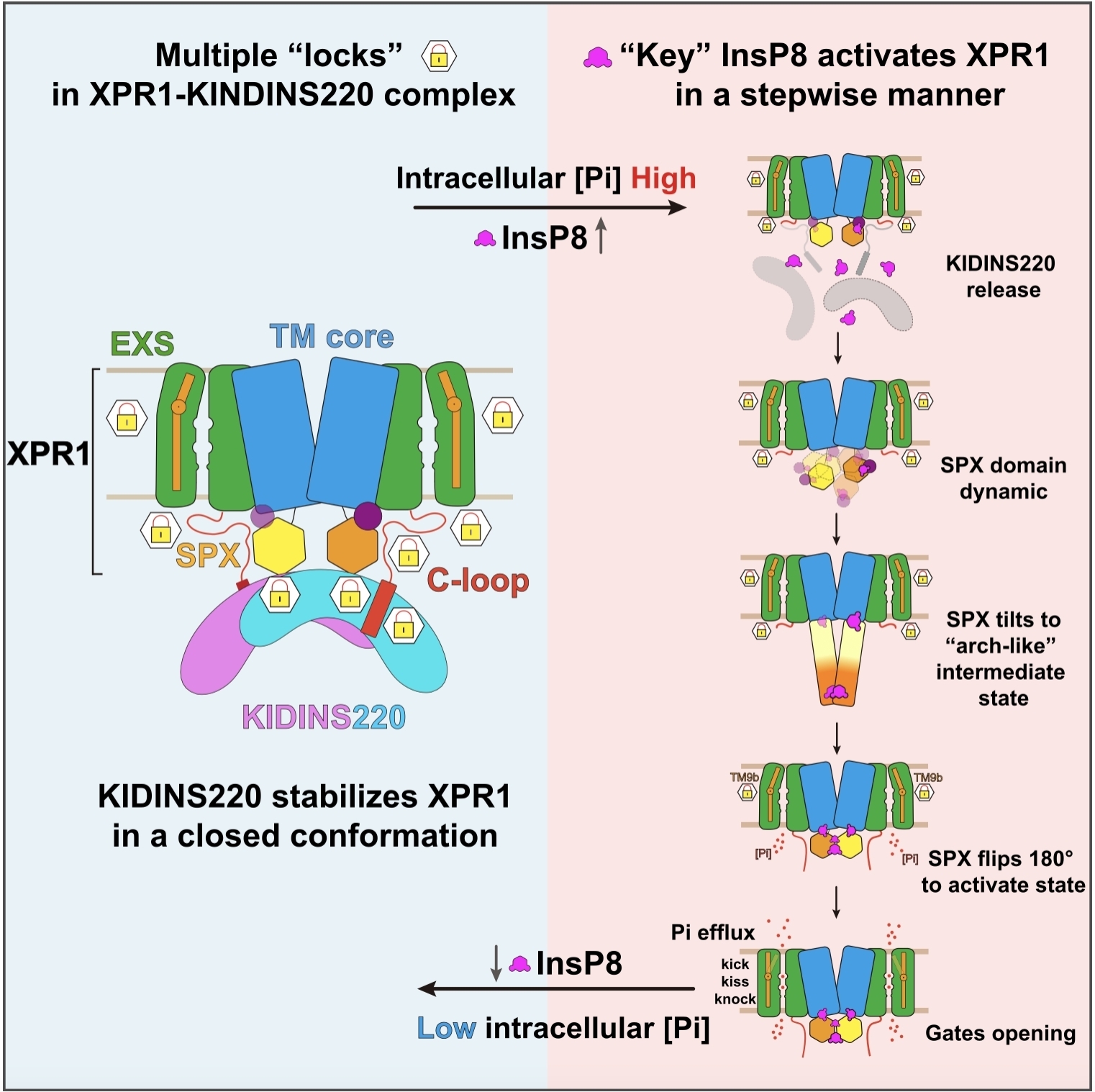
图2.KIDINS220和InsP8调控XPR1磷酸盐转运活性的模型
总体来讲,本研究完整描绘了XPR1的逐步激活过程,并提出了两个新颖模型:“key-to-locks”揭示了InsP8如何解除KIDINS220及XPR1自身施加的多重抑制,“knock–kiss–kick”描述了磷酸盐的外排过程(图2)。这些发现不仅为理解人类磷酸盐稳态提供了分子基础,也为脑钙化、肿瘤等疾病的致病机理研究及潜在干预策略开辟了新方向。
中国科学院上海有机化学研究所生物与化学交叉研究中心博士研究生王晓捷、柏忠谏,澳大利亚国立大学博士研究生Ciara Wallis为共同第一作者。张一小研究员, Ben Corry教授, 孙亚东教授, Stephen Shears教授为本文通讯作者。第二军医大学杨田教授、杭州师范大学雷明光教授以及本文其他作者亦做出了重要贡献。该工作得到了科技部科技创新2030-“脑科学与类脑研究”重大项目、国家自然科学基金海外优青项目、中国科学院上海分院青年英才培育计划以及上海市科委的资助。
张一小研究员长期招聘细胞生物学、药物化学、生物化学和结构生物学方向博士后和科研助理,欢迎申请(yzhang@@@sioc.ac.cn)。
原文链接:https://doi.org/10.1016/j.molcel.2025.08.003
参考文献:
1. Lopez-Sanchez, U., et al., Characterization of XPR1/SLC53A1 variants located outside of the SPX domain in patients with primary familial brain calcification. Sci Rep, 2019. 9(1): p. 6776.
2. Li, X., et al., Control of XPR1-dependent cellular phosphate efflux by InsP(8) is an exemplar for functionally-exclusive inositol pyrophosphate signaling. Proc Natl Acad Sci U S A, 2020. 117(7): p. 3568–3574.
3. Bondeson, D.P., et al., Phosphate dysregulation via the XPR1-KIDINS220 protein complex is a therapeutic vulnerability in ovarian cancer. Nat Cancer, 2022. 3(6): p. 681–695.
4. Orimo, K., et al., A Japanese family with idiopathic basal ganglia calcification carrying a novel XPR1 variant. J Neurol Sci, 2023. 451: p. 120732.
